5.1.1. Exprimarea concentraţiei soluţiilor
În practică se utilizează mai multe moduri de exprimare a concentraţiei soluţiilor:
a) Concentraţia procentuală, c%, (% de masă) arată numărul de grame de substanţă dizolvată, md, în 100 g de soluţie, ms; în cazul sistemelor disperse gazoase concentraţia se exprimă de obicei în % de volum. Acest mod de exprimare arată numărul de volume de substanţă, Vd, dizolvate în 100 de volume de soluţie, Vs. Aerul este un amestec gazos cu compoziţia volumică: 78% N2, 20,8% O2 şi restul gaze aerogene şi gaze accidentale.
![]() sau, pentru amestecuri gazoase:
sau, pentru amestecuri gazoase:
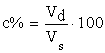 (5.2)
(5.2)
b) Concentraţia molară (m, M, cm) arată numărul de moli de substanţă dizolvată, nd, într-un litru (1dm3, 1000ml) de soluţie, Vs. Exprimând volumul soluţiei în litri, pentru o substanţă cu masa moleculară Md, expresia după care se poate calcula concentraţia molară, este:
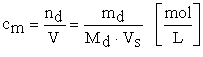 (5.3)
(5.3)
Soluţia care conţine într-un litru, 1 mol de substanţă dizolvată se numeşte soluţie molară (sau 1m), cea care conţine 2 moli de substanţă se numeşte soluţie 2 m sau dublu molară, cea care conţine 0,1 moli se numeşte soluţie 0,1m sau decimolară.
c) Concentraţia normală (n, N, cn) arată numărul de echivalenţi gram, nE, de substanţă dizolvată într-un litru de soluţie, Vs. Exprimând volumul soluţiei în litri, pentru o substanţă cu echivalentul gram E, expresia după care se poate calcula concentraţia normală, este:
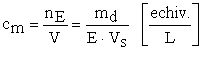 (5.4)
(5.4)
d) Concentraţia molală (b, cM) arată numărul de moli de substanţă dizolvată în 1000g de dizolvant:
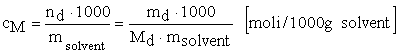 (5.5)
(5.5)
La fel ca şi în cazul exprimării concentraţiei molare, concentraţiile normale şi molale pot exprima multiplii sau submultiplii de echivalenţi gram respectiv de moli dintr-un litru de soluţie.
e) Fracţia molară (X, Y) reprezintă raportul dintre numărul de moli ai unui component dintr-un amestec, ni şi numărul total de moli din sistem, nt.
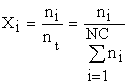 (5.6)
(5.6)
În orice sistem suma fracţiilor molare ale tuturor componenţilor este egală cu unitatea. Aceasta este condiţia de normare a fracţiilor molare:
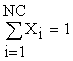 (5.7)
(5.7)
f) Titrul (T) arată numărul de grame de substanţă dizolvată, md, într-un mililitru de soluţie, Vs:
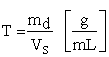 (5.8)
(5.8)
Trecerea de la concentraţia molară sau normală la titru se face utilizând relaţiile de echivalenţă a concentraţiilor:
![]() (5.9)
(5.9)